Suplementacja folianami u kobiet w ciąży i niemowląt – zalecenia i stanowisko PTGiP
Spis treści:
- Znaczenie folianów w ciąży i okresie połogu
1.1. Foliany w ciąży – znaczenie
1.2. Foliany w okresie połogu - Biochemia folianów i metabolizm
2.1. Mechanizm działania folianów: synteza DNA, metylacja, homocysteina
2.2. Aktywne foliany a kwas foliowy
2.3. UMFA – co to jest i jakie ma znaczenie kliniczne?
2.4. Kwas pteroilomonoglutaminowy – definicja, role - Wskazania i zalecenia dotyczące suplementacji
3.1. Rekomendacje w okresie ciąży – dawki, formy (kwas foliowy vs. 5-MTHF)
3.2. Potrzeby organizmu w okresie połogu – jak zmienia się metabolizm folianów? - Produkty bogate w foliany
- Fizjologiczne zapotrzebowanie na foliany po okresie prenatalnym
- Kwas foliowy i aktywne foliany w preparatach do żywienia niemowląt
- Czy foliany są kluczowym składnikiem diety niemowlęcia?
Znaczenie folianów w ciąży i okresie połogu
Ze względu na fundamentalną rolę w syntezie DNA oraz innych kluczowych składników komórek, odpowiednia podaż folianów jest niezbędna przez całe życie, a w szczególności w okresach szybkiego wzrostu komórek.
W ciąży zapotrzebowanie na foliany wzrasta. Niski poziom folianów w przypadku kobiet ciężarnych skorelowany jest z podwyższonym ryzykiem niekorzystnych wyników ciąży takich, jak:
- wady cewy nerwowej,
- przedwczesne odklejenie łożyska,
- przedwczesny poród,
- mała masa urodzeniowa noworodka.
Z kolei niedobór folianów w okresie niemowlęcym jest związany ze spowolnionym tempem wzrastania.
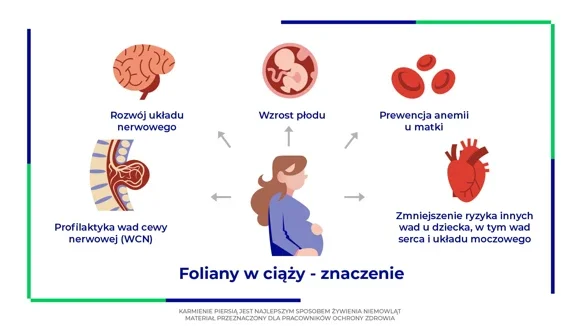
Foliany w ciąży – znaczenie
- profilaktyka wad cewy nerwowej (WCN) – odpowiedni poziom folianów w pierwszych tygodniach ciąży jest kluczowy do prawidłowego zamknięcia cewy nerwowej, zapobiegając ciężkim wadom, takim jak rozszczep kręgosłupa czy przepuklina mózgowo-rdzeniowa; badania naukowe wykazały, że właściwe spożycie folianów w okresie przedkoncepcyjnym i we wczesnym okresie ciąży może zredukować ryzyko wystąpienia wad cewy nerwowej nawet o 70%,
- wzrost płodu – jako niezbędne koenzymy w licznych szlakach metabolicznych, foliany biorą udział w syntezie DNA, metabolizmie aminokwasów, a także podziale komórek, dzięki czemu odgrywają kluczową rolę w procesie rozwoju i wzrostu komórek u rozwijającego się płodu,
- rozwój układu nerwowego – foliany pełnią ważną rolę w prawidłowym kształtowaniu ośrodkowego układu nerwowego (OUN) płodu, wpływając na szybko dzielące się komórki nerwowe w rozwijającym się mózgu,
- prewencja anemii u matki – odpowiednia podaż zapobiega rozwojowi niedokrwistości megaloblastycznej wśród kobiet ciężarnych, która jest szczególnie niebezpieczna w przebiegu ciąży,
- zmniejszenie ryzyka innych wad u dziecka, w tym wad serca i układu moczowego, rozszczepu wargi i podniebienia czy zespołu Downa.
Foliany w okresie połogu
Odpowiednia podaż folianów w okresie połogu pozwala zapobiec przed wyczerpaniem rezerw i rozwojem niedoboru folianów po porodzie. Optymalne wysycenie organizmu kobiety wspomaga produkcję pokarmu bogatego w foliany, które są krytyczne dla utrzymania odpowiedniego tempa wzrostu noworodka i jego dalszego rozwoju.
Biochemia folianów i metabolizm
Foliany to ogólne określenie grupy związków, do których należy naturalnie występująca w żywności witamina B9 oraz jej syntetyczna forma – kwas foliowy (kwas pteroilomonoglutaminowy).
Cykl kwasu foliowego warunkuje przebieg kluczowych procesów, takich jak metabolizm kwasów nukleinowych i aminokwasów, a także proliferacja i różnicowanie komórek. Z tego względu zachowanie homeostazy w obrębie przemian folianów stanowi fundament fizjologicznego rozwoju płodu.
Absorpcja naturalnie występujących folianów zachodzi przede wszystkim w proksymalnym odcinku jelita cienkiego (dwunastnicy i jelicie czczym). Wskutek kaskady przemian biochemicznych powstaje główna, aktywna metabolicznie postać kwasu foliowego, czyli 5-metylotetrahydrofolian (5-MTHF), który może być bezpośrednio zaangażowany w wewnątrzkomórkowe szlaki biologiczne.
Mechanizm działania folianów: synteza DNA, metylacja, homocysteina
Przebieg szlaku metabolicznego folianów jest niezbędny do utrzymania procesów, takich jak:
- przemiany homocysteiny – podwyższony poziom homocysteiny stanowi czynnik ryzyka wystąpienia incydentów sercowo-naczyniowych oraz schorzeń neurodegeneracyjnych i psychiatrycznych,
- biosynteza puryn i pirymidyn, warunkująca prawidłową syntezę kwasów nukleinowych (DNA i RNA),
- metylacja DNA, RNA oraz białek histonowych, determinująca odpowiednią ekspresję genów, stabilność genomu oraz prawidłowe różnicowanie komórek.
Następstwem właściwych przemian folianów jest metylacja DNA i białek. Proces ten napędzany jest przez remetylację homocysteiny do metioniny, która ulega dalszej konwersji do S-adenozylometioniny (SAM) – podstawowego donora grup metylowych. Odpowiedni
wzorzec metylacji kwasów nukleinowych i struktur białkowych stanowi warunek prawidłowego kształtowania zarodka i płodu.
Aktywne foliany a kwas foliowy
Podstawowa różnica wynika z biodostępności i konieczności biotransformacji. Kwas foliowy jest formą syntetyczną, utlenioną i nieaktywną biologicznie, która wymaga wieloetapowego procesu przemian z udziałem enzymu reduktazy dihydrofolianowej (DHFR), którego wydajność u ludzi jest niska i łatwo ulega wysyceniu.
Z kolei sól wapniowa 5-MTHF jest aktywną formą folianów, tożsamą z naturalnie występującą w organizmie. Wyróżnia ją wyższa biodostępność i większe tempo wysycenia organizmu. Nie wymaga aktywacji przez DHFR ani enzymu reduktazy metylenotetrahydrofolianowej (MTHFR), dzięki czemu omija tzw. pułapkę folianową. Jest również skuteczna niezależnie od polimorfizmów genu MTHFR, a także zmniejsza ryzyko skorelowane z nagromadzeniem niezmetabolizowanego kwasu foliowego (UMFA).
W przeciwieństwie do 5-MTHF, który stanowi dominującą formę folianów w pożywieniu (w tym w mleku kobiecym), kwas foliowy jest utlenioną postacią niewystępującą w naturze.
Tabela 1. Aktywne foliany a kwas foliowy – jaka jest różnica?
| 5-MTHF | Kwas foliowy |
| Występuje naturalnie w osoczu I erytrocytach, osoczu pępowinowym oraz mleku kobiecym | Stosowany w suplementach diety i żywności fortyfikowanej |
| Biologicznie aktywna forma folianów | Syntetyczna, utleniona forma folianów |
| Wysoka biodostępność | Nie wykazuje aktywności biologicznej |
| Nie wymaga wieloetapowych przemian, wchodzi bezpośrednio w cykl folianów | Wymaga wieloetapowych przemian metabolicznych, aby wejść do cyklu folianowego |
| Metabolizm i przemiany niezależnie od genotypu pacjenta | U osób z mutacją genu MTHFR zaburzone przekształcanie do jego aktywnej formy |
| Nie wyznaczono górnego tolerowanego poziomu spożycia (UL) | Górny tolerowany poziom spożycia (UL) dla osób dorosłych oraz kobiet ciężarnych i karmiących wynosi 1000 µg/dobę |
| Brak ryzyka maskowania niedoborów wit. B12 | Zbyt wysokie dawki mogą maskować niedobory wit. B12, opóźniając diagnozę niedokrwistości megaloblastycznej |
| Brak narażenia kobiet i dzieci na konsekwencje zespołu UMFA | Ryzyko związane z nagromadzeniem UMFA |
UMFA – co to jest i jakie ma znaczenie kliniczne?
UMFA (z ang. Unmetabolized Folic Acid) to niezmetabolizowany kwas foliowy, który pojawia się w krwioobiegu, gdy podaż kwasu foliowego przekracza zdolności metaboliczne organizmu, a w szczególności wydajność enzymu DHFR.
Obecność i kumulacja niezmetabolizowanego kwasu foliowego wywiera efekt hamujący na reduktazę dihydrofolianową, co blokuje redukcję kwasu foliowego do dihydrofolianu i uniemożliwia jego dalsze przemiany. Co istotne, UMFA jest również silnym inhibitorem kluczowego enzymu reduktazy metylenotetrahydrofolianowej. Spadek jej aktywności zaburza cały cykl folianowy, prowadząc do hiperhomocysteinemii, upośledzenia syntezy puryn i pirymidyn oraz deregulacji procesów metylacji.
Kwas pteroilomonoglutaminowy – definicja, role
Kwas pteroilomonoglutaminowy (powszechnie określany jako kwas foliowy, z ang. Folic Acid – FA) to utleniona, rozpuszczalna w wodzie, syntetyczna forma witaminy B9. W przeciwieństwie do naturalnie występujących folianów, forma ta nie jest spotykana w przyrodzie. W organizmie pełni rolę prekursora, który dopiero po redukcji do tetrahydrofolianu może wejść w szlaki metaboliczne.
Ze względu na swoją wysoką stabilność, biodostępność oraz niskie koszty produkcji, jest to główna postać witaminy B9 wykorzystywana powszechnie w suplementach diety oraz fortyfikowanej żywności.
Wskazania i zalecenia dotyczące suplementacji
Zależnie od wyjściowej stratyfikacji ryzyka wystąpienia wad płodu, w suplementacji folianami kobiet w ciąży i w czasie laktacji, a także przed planowanym poczęciem, dopuszcza się stosowanie syntetycznego kwasu foliowego, aktywnej postaci 5-MTHF bądź preparatów łączonych. Należy jednocześnie podkreślić, że w stanach niedoborowych, celem prawidłowego funkcjonowania cyklu przemian folianów, rekomenduje się równoległą suplementację choliny, a także witamin B6 i B12.
Głównym wskazaniem do suplementacji w okresie przedkoncepcyjnym i wczesnej ciąży jest profilaktyka wad cewy nerwowej, do której zamknięcia dochodzi w pierwszych 28 dniach po zapłodnieniu. Odpowiednia podaż folianów wspiera również dalszy rozwój i wzrastanie płodu, zmniejsza ryzyko hiperhomocysteinemii i związanych z nią powikłań położniczych (np. małej masy urodzeniowej noworodka), a także obniża ryzyko wystąpienia u potomstwa m.in. autyzmu czy zespołu Downa.
Rekomendacje w okresie ciąży – dawki, formy (kwas foliowy vs. 5-MTHF)
Zgodnie z najnowszymi rekomendacjami Polskiego Towarzystwa Ginekologów i Położników (PTGiP) w zakresie suplementacji folianów w okresie przedkoncepcyjnym, ciąży i połogu, z 2024 roku, dawkowanie oraz forma folianów zależą od stopnia ryzyka wystąpienia wad płodu.
- Grupa niskiego ryzyka (zdrowe kobiety, wywiad nieobciążony): – w okresie przedkoncepcyjnym zaleca się 400 µg kwasu foliowego lub 400 µg 5-MTHF i 400 µg kwasu foliowego dziennie, – w pierwszym trymestrze ciąży zaleca się 400-800 µg 5-MTHF dziennie lub podaż łączoną (kwas foliowy i aktywny folian), – w II i III trymestrze ciąży rekomendowana dzienna dawka to 600-800 µg 5-MTHF lub forma łączona.
- Grupa pośredniego ryzyka (wywiad obciążony, m.in. cukrzyca przedciążowa, otyłość, choroby układu pokarmowego, stosowanie leków przeciwpadaczkowych, używki): – w okresie przedkoncepcyjnym zaleca się suplementację 400 µg kwasu foliowego lub 400 µg 5-MTHF i 400 µg kwasu foliowego dziennie, – w czasie ciąży i laktacji zaleca się dawkę 800 µg na dobę, preferencyjnie w formie 5-MTHF lub preparatów łączonych, – wyjątkiem są pacjentki z otyłością (BMI >30 kg/m²), u których po stwierdzeniu niskiego stężenia folianów (<28 nmol/l) rekomenduje się 5 mg folianów na dobę (wraz z mio-inozytolem), maksymalnie do 12. tygodnia ciąży.
- Grupa wysokiego ryzyka (wady cewy nerwowej w wywiadzie): – przed planowanym poczęciem wymagana jest suplementacja 5 mg kwasu foliowego na dobę, – w okresie ciąży i laktacji dawkowanie zmienia się na 800 µg 5-MTHF dziennie lub w dawkach łączonych.
Potrzeby organizmu w okresie połogu – jak zmienia się metabolizm folianów?
W okresie połogu i karmienia piersią zapotrzebowanie organizmu na foliany pozostaje wysokie. Ich zawartość w mleku kobiecym jest ściśle regulowana, bez wpływu na poziom folianów u matki (wyjątek stanowi ich kliniczny niedobór).
Stężenie folianów w krwiobiegu matki spada w trakcie laktacji, natomiast wzrasta w krwiobiegu niemowlęcia. W efekcie, wydzielanie folianów do mleka może prowadzić do znacznego spadku ich stężenia u kobiety karmiącej. W związku z tym, głównym celem suplementacji folianów w trakcie laktacji jest zaspokojenie zwiększonego zapotrzebowania organizmu matki, ze względu na dostarczanie folianów wraz z mlekiem, a także zapobieganie niedoborowi.
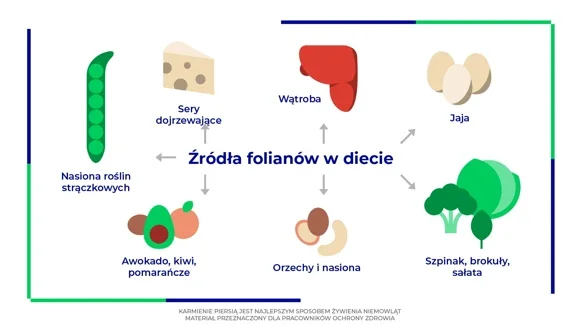
Produkty bogate w foliany
Najlepszym źródłem naturalnych folianów w diecie są ciemnozielone warzywa liściaste, zwłaszcza w surowej postaci (np. szpinak, brokuły, sałata) oraz nasiona roślin strączkowych.
Foliany występują również w produktach pochodzenia zwierzęcego, takich jak:
- jaja,
- wątroba,
- sery dojrzewające.
Oprócz folianów naturalnie występujących w pożywieniu, źródłem tej witaminy może być również żywność fortyfikowana. Syntetyczny kwas foliowy jest w wielu krajach powszechnie dodawany m.in. do białej mąki pszennej czy produktów zbożowych. W ujęciu globalnym najpowszechniejszą strategią profilaktyki pozostaje obligatoryjna fortyfikacja mąki, którą zaimplementowano w ponad 80 krajach.
Fizjologiczne zapotrzebowanie na foliany po okresie prenatalnym
Zapotrzebowanie na foliany po zakończeniu okresu prenatalnego zmienia się w zależności od aktualnego etapu rozwoju dziecka oraz stanu fizjologicznego matki.
W okresie połogu i laktacji organizm kobiety wciąż wymaga zwiększonej podaży tego składnika. Kontynuacja suplementacji w tym czasie jest szczególnie ważna dla wsparcia prawidłowego funkcjonowania organizmu matki, a także dostarczania folianów do pokarmu naturalnego, co warunkuje prawidłowy rozwój niemowlęcia.W przypadku niemowląt do 6 miesięcy, zapotrzebowanie szacuje się na 65 µg folianów dziennie. Mleko zdrowej matki jest w stanie pokryć te potrzeby. W przypadku braku możliwości karmienia piersią, preparaty do żywienia niemowląt są odpowiednio fortyfikowane kwasem foliowym, w stężeniach odpowiadających naturalnie występującym folianom w mleku kobiecym. Dla niemowląt w wieku 7-12 miesięcy zalecane dzienne spożycie folianów rośnie do 80 µg. Na tym etapie foliany powinny być również dostarczane w ramach rozszerzania diety (np. poprzez puree z gotowanych warzyw, owsiankę z mlekiem, a później pieczywo).
Kwas foliowy i aktywne foliany w preparatach do żywienia niemowląt
W preparatach do żywienia niemowląt stosowane są obecnie dwie formy folianów – syntetyczny kwas foliowy oraz aktywne foliany.
- Syntetyczny kwas foliowy – tradycyjna postać witaminy B9. Większość folianów obecnych w preparatach do żywienia niemowląt, które stanowią wyłączne źródło pożywienia dla niemowląt karmionych sztucznie, występuje właśnie w formie dodanego kwasu foliowego.
- Aktywne foliany (L-metylofolian wapnia/L-5-MTHF-Ca) – w 2018 roku złożono wniosek o rozszerzenie dopuszczenia L-5-MTHF-Ca do stosowania w żywności dla niemowląt. Europejski Urząd ds. Bezpieczeństwa Żywności (EFSA) wydał pozytywną opinię, w której potwierdził, że L-metylofolian wapnia stanowi źródło folianów, które są biodostępne i bezpieczne w proponowanych zastosowaniach dla niemowląt i małych dzieci. W związku z tym, na mocy rozporządzenia delegowanego Komisji (UE) 2021/571, L-metylofolian wapnia został oficjalnie wpisany na listę substancji dozwolonych do dodawania jako źródło folianów w preparatach do początkowego i dalszego żywienia niemowląt, żywności dla dzieci oraz w przetworzonych produktach zbożowych.
Czy foliany są kluczowym składnikiem diety niemowlęcia?
Foliany pełnią kluczową rolę w prawidłowym rozwoju płodu oraz intensywnie rozwijającego się organizmu niemowlęcia. Dlaczego foliany odgrywają tak fundamentalną rolę na tym etapie życia?
- podziały komórkowe i intensywny wzrost tkanek – foliany są niezbędne do syntezy puryn i pirymidyn, co bezpośrednio warunkuje produkcję kwasów nukleinowych (DNA i RNA) we wszystkich rosnących komórkach,
- rozwój układu nerwowego – aktywna forma folianów (L-5-MTHF) dostarcza grup jednowęglowych niezbędnych do syntezy mieliny, neuroprzekaźników oraz fosfolipidów błonowych, które stanowią niezbędne elementy do prawidłowego dojrzewania i funkcjonowania mózgu oraz całego układu nerwowego,
- produkcja czerwonych krwinek – w okresie niemowlęcym foliany są niezbędne do szybkiej produkcji czerwonych krwinek; ich rola jest szczególnie ważna zwłaszcza w przypadku niemowląt urodzonych przedwcześnie, które mają bardzo ograniczone zapasy tego składnika, a ich intensywny wzrost może zwiększać zapotrzebowanie, co czyni je szczególnie podatnymi na ryzyko rozwoju niedoboru folianów.
FAQ
Czy badanie stężenia folianów w surowicy lub erytrocytach jest przydatne w rutynowej ocenie pacjentki planującej ciążę?
Zgodnie z aktualnymi wytycznymi, rutynowe oznaczanie stężenia folianów u wszystkich pacjentek planujących ciążę nie jest rekomendowane. Złotym standardem pozostaje uniwersalna profilaktyka (suplementacja) w populacji ogólnej. Badanie poziomu folianów warto natomiast rozważyć u pacjentek z grup podwyższonego ryzyka niedoborów, takich jak kobiety z zaburzeniami wchłaniania (np. celiakia, stan po operacji bariatrycznej), stosujące przewlekle leki obniżające stężenie folianów (np. leki przeciwpadaczkowe) czy pacjentki z chorobą otyłościową.
Kiedy warto rozważyć badanie polimorfizmów genu MTHFR przed doborem formy folianu?
Zgodnie z aktualnym stanowiskiem PTGiP (2024), oznaczanie polimorfizmów genu MTHFR wśród kobiet planujących ciążę oraz ciężarnych nie jest uzasadnione klinicznie. Wybór aktywnych folianów (5-MTHF) pozwala na ominięcie szlaku enzymatycznego zależnego od tego genu, co czyni go skutecznym rozwiązaniem dla wszystkich pacjentek, bez konieczności diagnostyki.
Czy są sytuacje, w których suplementacja folianami w dawkach standardowych jest przeciwwskazana lub wymaga modyfikacji?
Tak, dawki standardowe wymagają modyfikacji w przypadku pacjentek obciążonych czynnikami ryzyka. Zgodnie z zaleceniami ekspertów PTGiP, kobiety w trakcie ciąży m.in. z obciążonym wywiadem, cukrzycą przedciążową, otyłością, niewydolnością wątroby, chorobami układu pokarmowego oraz pacjentki z obniżoną aktywnością MTHFR, a także przyjmujące niektóre leki (np. przeciwpadaczkowe czy metotreksat), zaliczane są do grupy pośredniego ryzyka i wymagają suplementacji 800 µg 5-MTHF na dobę lub w dawkach łączonych. W przypadku suplementacji u kobiet w grupie wysokiego ryzyka, u których w wywiadzie potwierdzono wady cewy nerwowej u matki, ojca lub ich potomstwa, dawkowanie w okresie przedkoncepcyjnym wzrasta do 5 mg syntetycznego kwasu foliowego na dobę.
Czy oznaczenie poziomu folianów w surowicy ma wartość kliniczną, czy lepiej oceniać foliany w erytrocytach?
Ocena folianów w erytrocytach jest znacznie bardziej wiarygodna z klinicznego punktu widzenia, ponieważ stanowi najlepszy wskaźnik długoterminowego spożycia. Stężenie folianów w surowicy jest czułym markerem, ale odzwierciedla jedynie bieżącą, krótkoterminową podaż folianów z dietą.
Czy istnieją różnice w zapotrzebowaniu na foliany pomiędzy ciążą pojedynczą a mnogą?
W przypadku ciąży wielopłodowej wymagania żywieniowe są fizjologicznie zwiększone, co ma bezpośredni wpływ na przebieg ciąży. Z tego względu standardowe zalecenia dedykowane ciąży pojedynczej wymagają specjalnego dostosowania. Dostarczane do organizmu foliany w ciąży wielopłodowej mają szczególne znaczenie – wskazuje się, że niedokrwistość spowodowana ich niedoborem występuje aż osiem razy częściej u matek w ciąży bliźniaczej w porównaniu do pojedynczej. Z tego powodu odpowiednia modyfikacja (najczęściej zwiększenie dawki) suplementacji kwasu foliowego przez kobiety w okresie ciąży mnogiej jest niezbędna do zabezpieczenia rezerw organizmu matki i wsparcia rozwoju płodów.
Bibliografia:
- Seremak-Mrozikiewicz A., Bomba-Opoń D., Drews K., Kaczmarek P., Wielgoś M., Sieroszewski P. Stanowisko Ekspertów Polskiego Towarzystwa Ginekologów i Położników w zakresie suplementacji folianów oraz warunków stosowania dodatkowej suplementacji choliny i witamin B6 i B12 w okresie przedkoncepcyjnym, ciąży i połogu. Ginekologia i Perinatologia Praktyczna 2024; 9(2): 154-156.
- Wang S, Wei J, Wang D, et al. The association between folic acid supplementation, maternal folate during pregnancy and intelligence development in infants: a prospective cohort study. Food Science and Human Wellness 2021; 10(2): 197-204.
- Lamers Y. Folate recommendations for pregnancy, lactation, and infancy. Ann Nutr Metab. 2011; 59(1): 32-37.
- Banyś K., Knopczyk M., Bobrowska-Korczak B. Znaczenie kwasu foliowego dla zdrowia organizmu człowieka. Farm Pol 2020; 76(2): 79-87.
- Krupa A, Skrzypulec-Plinta V. Active folates and choline in prenatal development: current recommendations and clinical implications. Ginekol Pol. Published online December 23, 2025.
- Makowska-Donajska M, Hirnle L. Suplementacja witamin i składników mineralnych podczas ciąży. Ginekologia i Perinatologia Praktyczna. 2017;2(4):166-172.
- Obeid, R., Warnke, I., Hecht, C., Troesch, B., Barbanti, L., Tanadini, M., & Koletzko, B. Dependence of bioavailability of folic acid and (6S)-5-methyltetrahydrofolate on baseline red blood cell folate concentrations in infants. Human Nutrition & Metabolism 2025; 42: 200335.
- Best KP, Green TJ, Sulistyoningrum DC, et al. Maternal Late-Pregnancy Serum Unmetabolized Folic Acid Concentrations Are Not Associated with Infant Allergic Disease: A Prospective Cohort Study. J Nutr. 2021;151(6):1553-1560.
- Obeid R, Warnke I, Bendik I, Troesch B, Schoop R, Chenal E, Koletzko B on behalf of the MEFOLIN Study Group. Infants’ Folate Markers and Postnatal Growth in the First 4 Months of Life in Relation to Breastmilk and Maternal Plasma Folate. Nutrients. 2023; 15(6):1495.
- Rychlik E., Stoś K., Woźniak A., Mojska H. (Eds.). 2024. Normy żywienia dla populacji Polski. Warszawa: Narodowy Instytut Zdrowia Publicznego PZH – Państwowy Instytut Badawczy.
- Patti MA, Braun JM, Arbuckle TE, MacFarlane AJ. Associations between folic acid supplement use and folate status biomarkers in the first and third trimesters of pregnancy in the Maternal-Infant Research on Environmental Chemicals (MIREC) Pregnancy Cohort Study. Am J Clin Nutr. 2022;116(6):1852-1863.
- Lohner S, Fekete K, Berti C, et al. Effect of folate supplementation on folate status and health outcomes in infants, children and adolescents: a systematic review. Int J Food Sci Nutr. 2012;63(8):1014-1020.
- EFSA Panel on Nutrition, Novel Foods and Food Allergens (NDA Panel), Turck D, Bohn T, et al. Scientific opinion on the tolerable upper intake level for folate. EFSA J. 2023;21(11):e08353.
- Rozporządzenie delegowane Komisji (UE) 2021/571 z dnia 20 stycznia 2021 r. zmieniające załącznik do rozporządzenia Parlamentu Europejskiego i Rady (UE) nr 609/2013 w odniesieniu do wykazu substancji, które można dodawać do preparatów do początkowego żywienia niemowląt i preparatów do dalszego żywienia niemowląt, żywności dla dzieci oraz produktów zbożowych przetworzonych. Pobrany 26.02.2026 r., z https://eur-lex.europa.eu/legal-content/PL/TXT/PDF/?uri=CELEX:32021R0571
- Troesch B, Demmelmair J, Gimpfl M, et al. Suitability and safety of L-5-methyltetrahydrofolate as a folate source in infant formula: A randomized-controlled trial. PLoS One. 2019;14(8):e0216790.
- Iglesias-Platas I, Sobczyńska-Malefora A, Ponnusamy V, Mahaveer A, Voong K, Nichols A, Dockery K, Holland N, Mulla S, Shearer MJ, et al. Serum Folate Concentrations in Exclusively Breastfed Preterm Infants Who Received No Supplementary Oral Folic Acid After Discharge: A Prospective Cohort Study. Nutrients. 2024; 16(23):4220.
- Goodnight W, Newman R; Society of Maternal–Fetal Medicine. Optimal nutrition for improved twin pregnancy outcome. Obstet Gynecol. 2009;114(5):1121-1134.
MOŻE CIĘ ZAINTERESOWAĆ...
MOŻE CIĘ RÓWNIEŻ ZAINTERESOWAĆ